18 августа 2023
Выводы учёных помогут в развитии новых способов борьбы с бактериями
Результаты исследования учёных из Сколтеха и научных центров в Швеции и Швейцарии помогли лучше понять, как устроено взаимодействие между бактериями и фагами – вирусами, которые заражают клетки бактерий. Открытие может стать важным этапом на пути развития новых способов борьбы с инфекциями. Работа опубликована в журнале Cell Reports.

Изображение 1.
Лабораторные эксперименты.
Автор: Александр Андриянов, аспирант Сколтеха, первый автор работы.
Микроорганизмы, вызывающие заболевания, становятся всё более устойчивыми к действию антибиотиков. Учёные по всему миру занимаются поиском новых способов борьбы с патогенными бактериями, один из которых – фаговая терапия. Бактериофаги – природные «хищники» и враги бактерий, которые обладают высокой специфичностью к распознаванию конкретных видов. Они безопасны для организма человека и имеют природное происхождение, а обнаружить их можно везде, где есть жизнь и бактерии. Фаги изучали ещё более ста лет назад, но вскоре интерес учёных к ним снизился из-за открытия антибиотиков.
«Наша лаборатория в Сколтехе занимается исследованием новых систем бактериального иммунитета. В последние годы биоинформатики предсказали очень много новых противовирусных систем и возникла практически целая область – микробная иммунология. Для большинства из этих систем не установлены молекулярные механизмы действия, поэтому один из способов понять, как работает микробный иммунитет, – это выяснить, как вирусы научились справляться с его действием. Взаимодействие между вирусами и бактериями можно сравнить с гонкой вооружений: когда у бактерий появляется новая стратегия защиты, она оказывает сильное давление на противоборствующую сторону – фаги. Можно ожидать, что скоро возникнут такие варианты фагов, которые научились каким-то образом противодействовать иммунитету бактерий. Это запускает новый этап адаптации со стороны бактерий, а такая активная конкуренция приводит к возникновению огромного разнообразия противовирусных систем»,– рассказывает руководитель Лаборатории анализа метагеномов и соавтор исследования Артём Исаев.
В работе учёные исследовали систему иммунитета BREX (от англ. bacteriophage exclusion) – защитный механизм бактерий в борьбе с фагами – и показали, что бактериофаг Т3 способен инфицировать BREX-культуру, только если экспрессирует специальный фермент – SAM-лиазу, разрушающий S-аденозилметионин, важный клеточный метаболит.
«SAM используется как донор метильных групп, которые могут регулировать экспрессию генов, а в случае BREX-системы метильная группа также служит меткой, позволяющей бактерии отличить собственную ДНК от неметилированной ДНК вируса. Однако оказалось, что как раз-таки метилирующая функция BREX не была затронута при экспрессии SAM-лиазы, в то время как BREX-защита была нарушена. Можно предположить, что SAM также является кофактором, необходимым для ингибирования вирусной инфекции BREX-системой»,– объясняет процедуру исследования Артём Исаев.
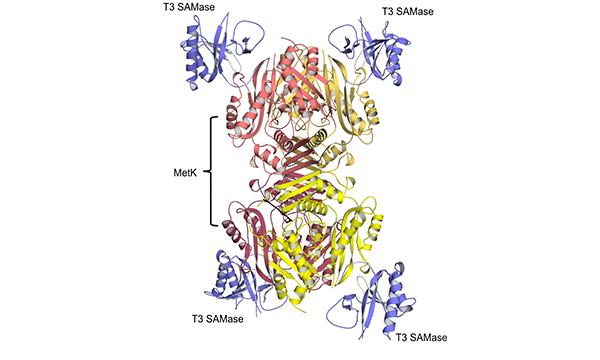 Изображение 2. Структура комплекса SAM-лиазы фага Т3 с SAM-синтазой E. coli. Автор: Артём Исаев.
Изображение 2. Структура комплекса SAM-лиазы фага Т3 с SAM-синтазой E. coli. Автор: Артём Исаев.
По словам исследователей, во многих странах уже создаются банки бактериофагов и развиваются проекты, позволяющие модифицировать вирусные частицы так, чтобы можно было сконструировать бактериофаг, эффективный против патогенного микроорганизма, обнаруженного в организме конкретного пациента.
«Мы всё ещё мало знаем о том, какие антизащитные белки кодируют фаги, но именно эти белки во многом определяют успешность заражения клеток бактерий в природных условиях, с учётом огромного разнообразия иммунных систем, обнаруживаемых в том числе и в патогенных бактериях. Наша работа вносит свой вклад в построение сети взаимодействий между вирусными антизащитными белками и системами бактериального иммунитета. Это необходимо будет учитывать на следующем этапе развития фаговой терапии, при создании фагов, способных целенаправленно уничтожать клетки „нежелательных” микроорганизмов»,– добавляет Артём Исаев.


