НМРЛ – немелкоклеточный рак легкого,
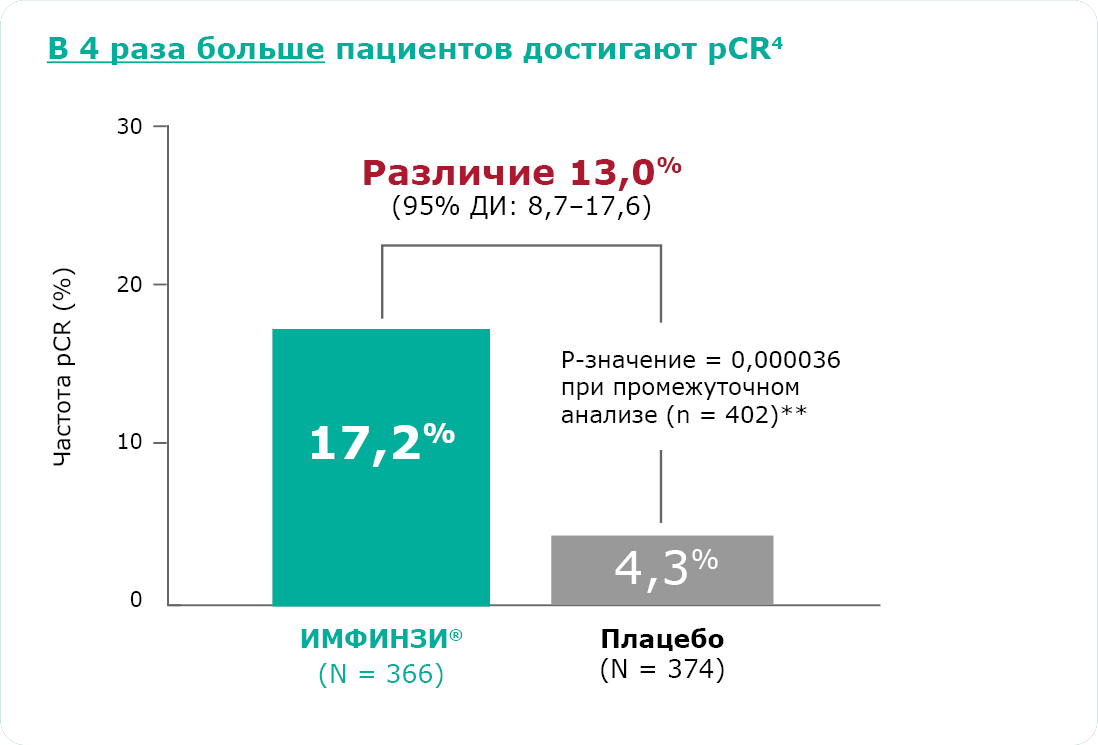
pCR – полный патоморфологический ответ,
ДИ – доверительный интервал,
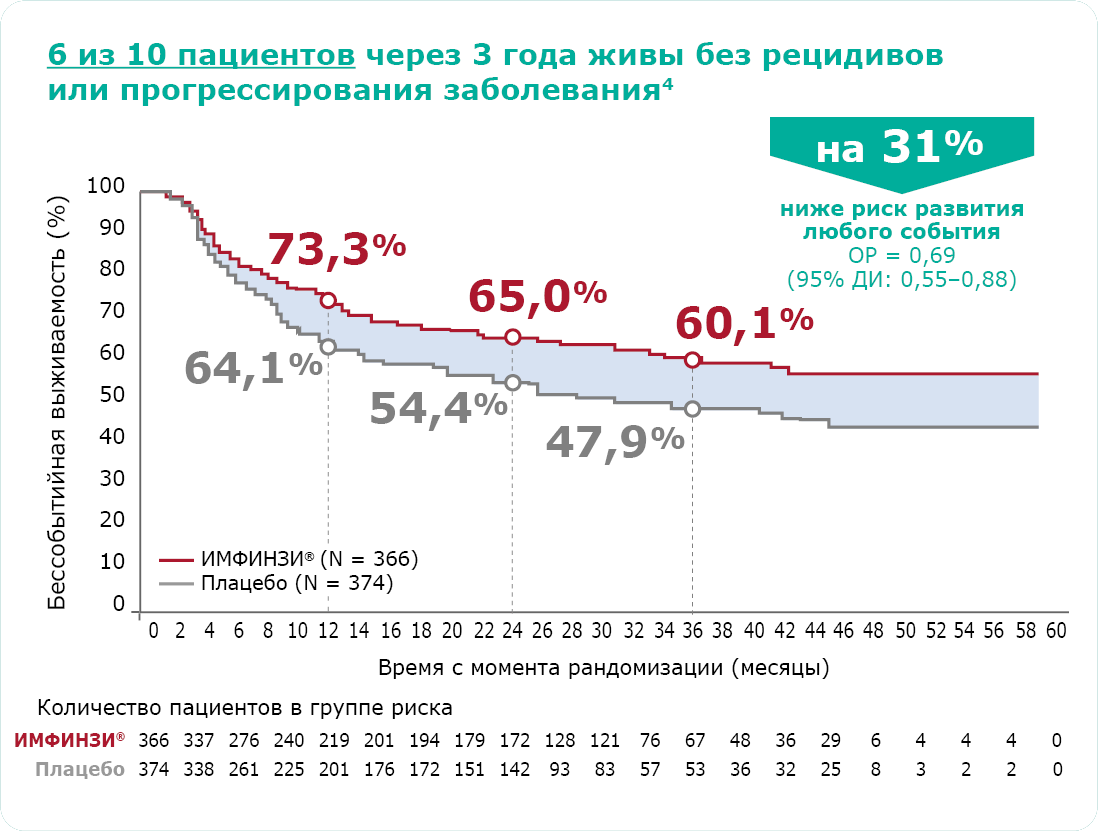
ОР – отношение рисков,
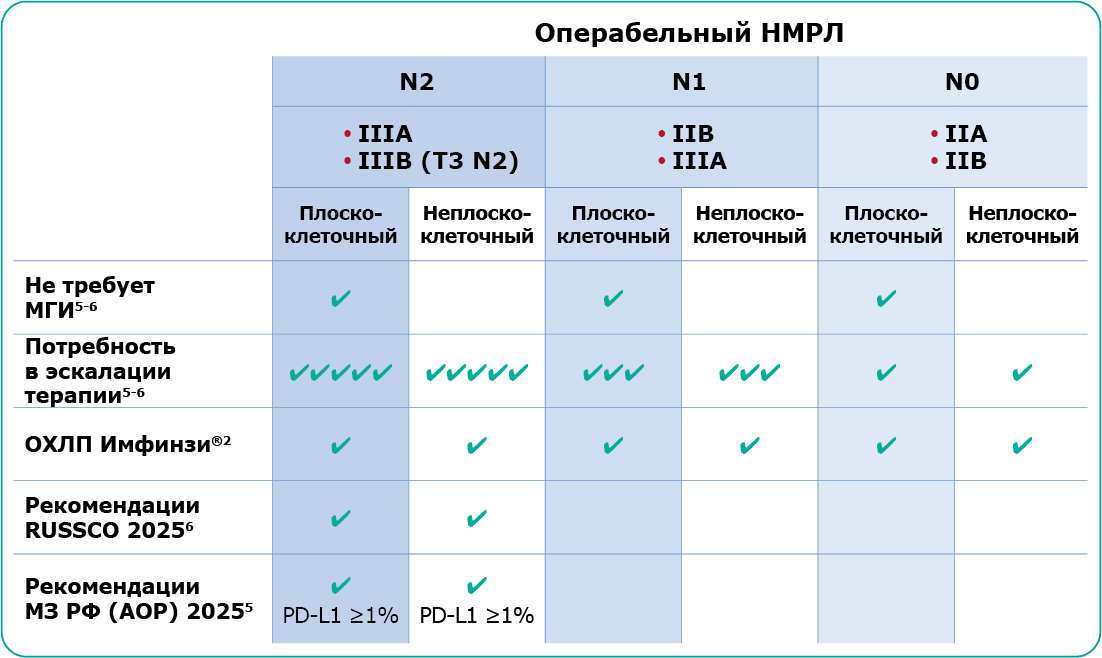
МГИ – молекулярно-генетическое исследование,
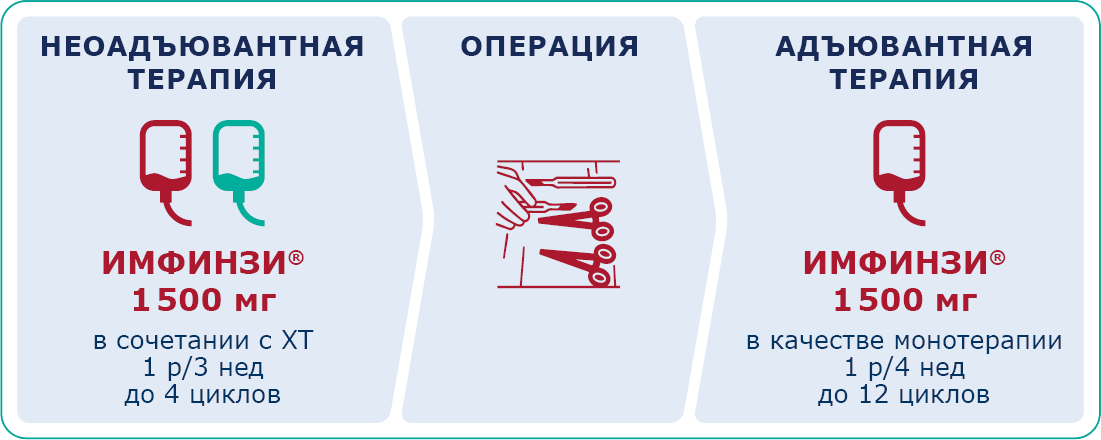
ХТ – химиотерапия.
|
1. ГРЛС. Электронный ресурс
https://grls.minzdrav.gov.ru/Default.aspx. Дата доступа: 02.02.2026.
2. Общая характеристика лекарственного препарата ИМФИНЗИ® (дурвалумаб), концентрат для приготовления раствора для инфузий, 50 мг/мл. Регистрационное удостоверение ЛП-№(009787)- (РГ-RU) от 30.12.2025
https://storage.yandexcloud.net/sb-prod-astrazeneca-static-01/ api/media/Imfinzi_ OKhLP.pdf. Дата доступа: 02.02.2026.
3. Clinicaltrial.gov/AEGEAN. Электронный ресурс:
https://www.clinicaltrials.gov/study/NCT03800134. Дата доступа: 02.02.2026.
4. Heymach JV, Harpole D, Mitsudomi T, et al. Perioperative durvalumab for resectable non–small-cell lung cancer. N Engl J Med. 2023;389(18):1672-1684 (Including Supplement and Protocol).
5. Клинические рекомендации. Злокачественное новообразование бронхов и легкого. АОР, ООО «РОКО» [электронный ресурс] Дата доступа: 27.01.2026. URL:
https://cr.minzdrav.gov.ru/view-cr/30_5.
6. Лактионов К. К., Артамонова Е. В., Бредер В. В. и соавт. Немелкоклеточный рак легкого. Клинические рекомендации RUSSCO, часть 1.1. Злокачественные опухоли 2025;15(3s2):90–132.
Материал предназначен для специалистов здравоохранения. Имеются противопоказания. При назначении ознакомьтесь, пожалуйста, с
полной общей характеристикой лекарственного препарата ИМФИНЗИ®.
Если Вам стало известно о нежелательной реакции при использовании лекарственного препарата «АстраЗенека», пожалуйста, сообщите эту информацию в медицинский отдел компании. Вы можете написать нам по электронной почте
Safety.Russia@astrazeneca.com, или связаться с нами по телефону 8 (495) 799-56-99, доб. 2580.
сли у Вас есть претензия в отношении качества или подлинности лекарственного препарата «АстраЗенека», пожалуйста, сообщите эту информацию в группу по качеству Компании: электронная почта:
productquality.ru@astrazeneca.com, телефон:
8 (495) 799-56-99, доб. 2580.
|
Номер одобрения: RU-27677
Дата одобрения: 10.02.2026
Дата истечения: 10.02.2028
|
ООО «АстраЗенека Фармасьютикалз»
Российская Федерация, 123112, Москва,
1-й Красногвардейский пр-д, д. 21, стр. 1
Телефон: +7 (495) 799 56 99
astrazeneca.ru
|

|
|